
丨本期分析丨
本期,药春秋(ID:bryaochunqiu)对厄贝沙坦进行调研分析,整理最新信息供大家参考。
丨简介丨
药理和适应症
ATC分类(解剖学治疗学及化学分类系统):
心血管系统 > 作用于肾素-血管紧张素系统的药物 > 血管紧张素II拮抗药
厄贝沙坦是血管紧张素II受体(AT1亚型)拮抗剂,通过与AT1血管紧张素II受体选择性的结合,以阻断血管紧张素II所引起的血管收缩和醛固酮分泌作用。
该药用于治疗成人原发性高血压,也可作为降压药物治疗方案的一部分,用于高血压和2型糖尿病成年患者的肾病治疗。
用法用量
推荐起始剂量为每次150 mg,每日1次,空腹或随餐服用均可。一般情况下,厄贝沙坦150mg每天一次比75mg能更好地控制24小时的血压。(从销售数据看,150mg规格销量远高于75mg规格。)
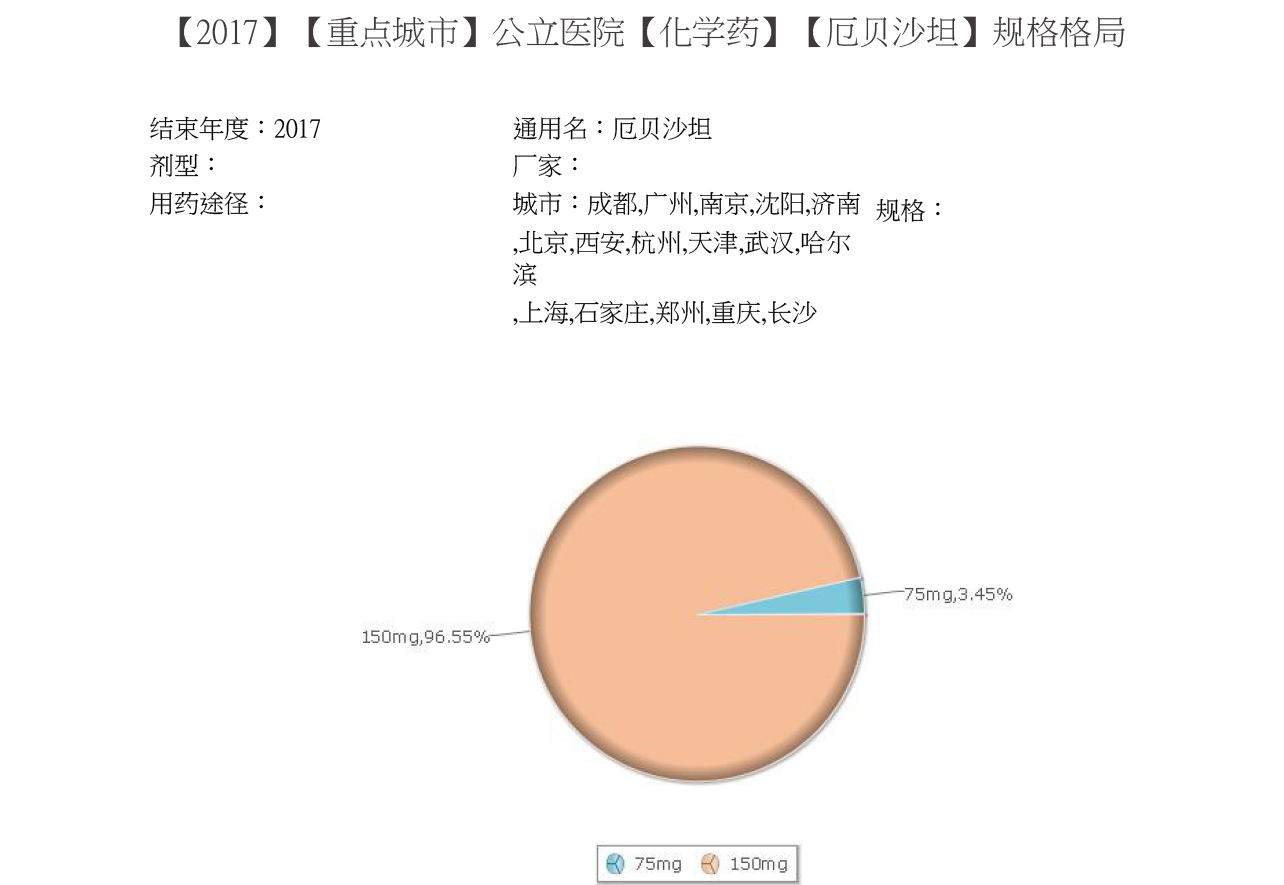
但对于特殊的病人:肾功能损伤、进行血液透析和年龄超过75岁的病人,初始剂量可考虑用75mg。
丨调研数据丨
国内批文数量
厄贝沙坦不属于289目录,
片剂国产批文12个,进口10个;
胶囊剂国产批文6个;
分散片国产批文4个。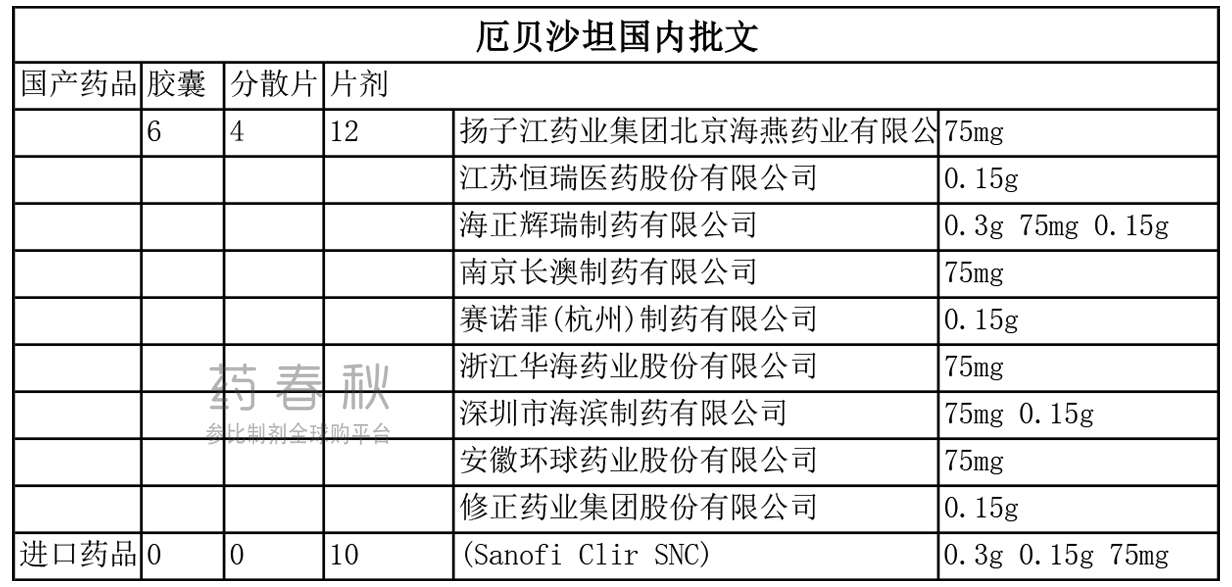
值得注意的是,拥有150mg规格批文的有:恒瑞医药、海正辉瑞、赛诺菲(杭州)、海滨制药、修正药业。尽管华海药业的75mg规格通过了一致性评价,但厄贝沙坦的大部分市场仍属于150mg规格的企业。
国内销售数据
米内网重点城市公立医院数据得到:
1. 厄贝沙坦2016年销售额总计:2.3亿元, 2017年前三季度销售额总计:1.7亿元;(图1)
2. 厄贝沙坦品牌格局:赛诺菲市场份额占83.12%,润都和恒瑞分别占4.47%和4.39(图2);
赛诺菲的厄贝沙坦片150mg销量最高,2017年前三季度销售1.4亿元;排第二的是润都制药额厄贝沙坦胶囊150mg(778万元);排第三的是恒瑞的厄贝沙坦片150mg(765万元)。(图3)
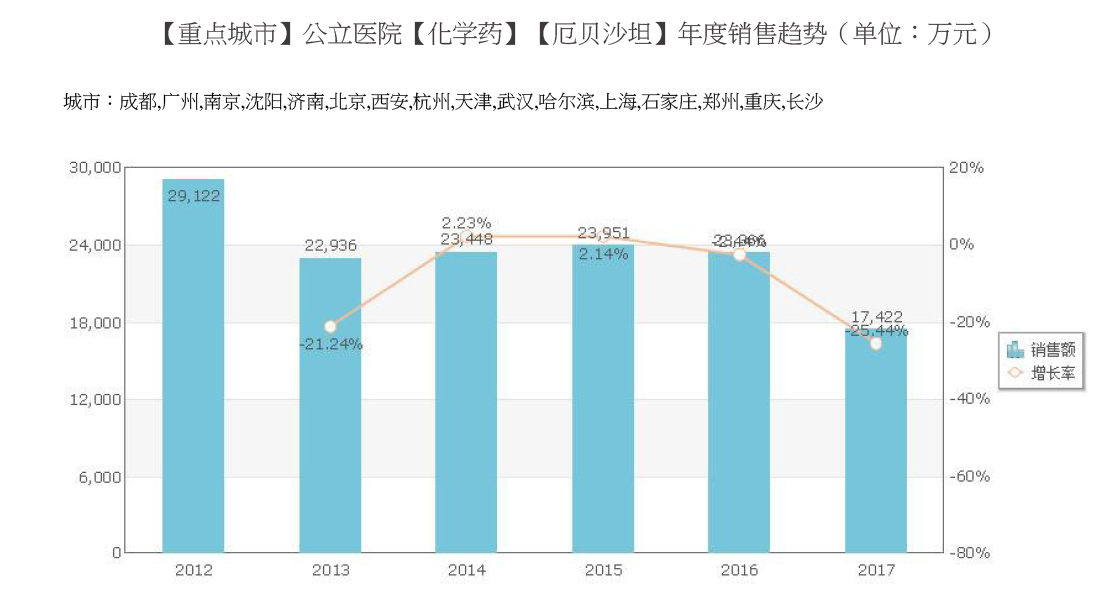
(图1)
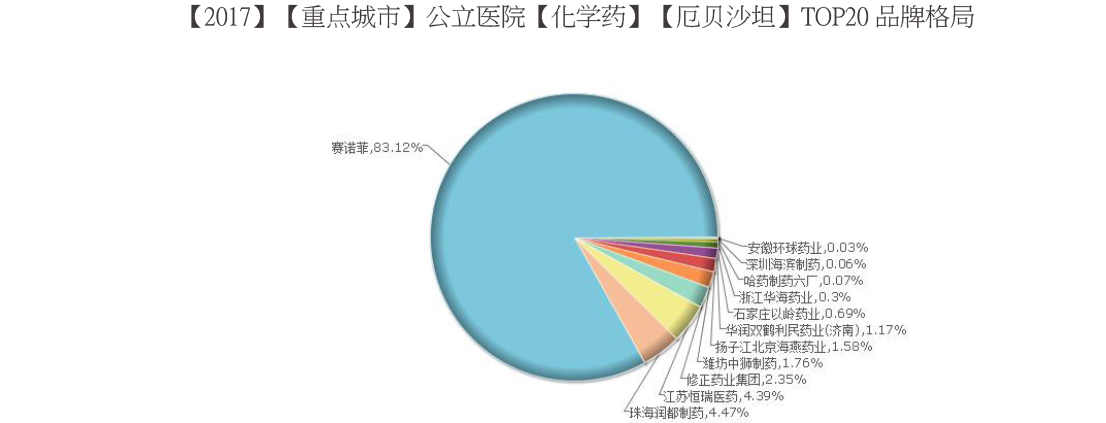 (图2)
(图2)
(图2)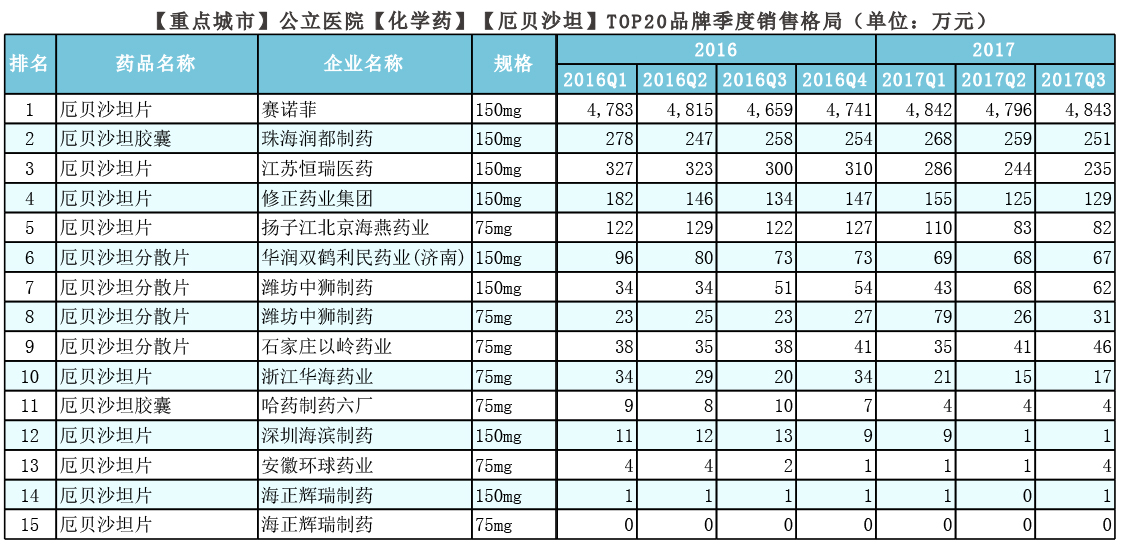
(图3)
国外上市情况
厄贝沙坦由赛诺菲(Sanofi)研发,首先于1997年8月27日获得欧洲药物管理局(EMA)批准,商品名Aprovel;之后于1997年9月30日获得美国食品药品管理局(FDA)批准,商品名Avapro;于2008年4月16日获得日本医药品医疗器械综合机构(PMDA)批准。
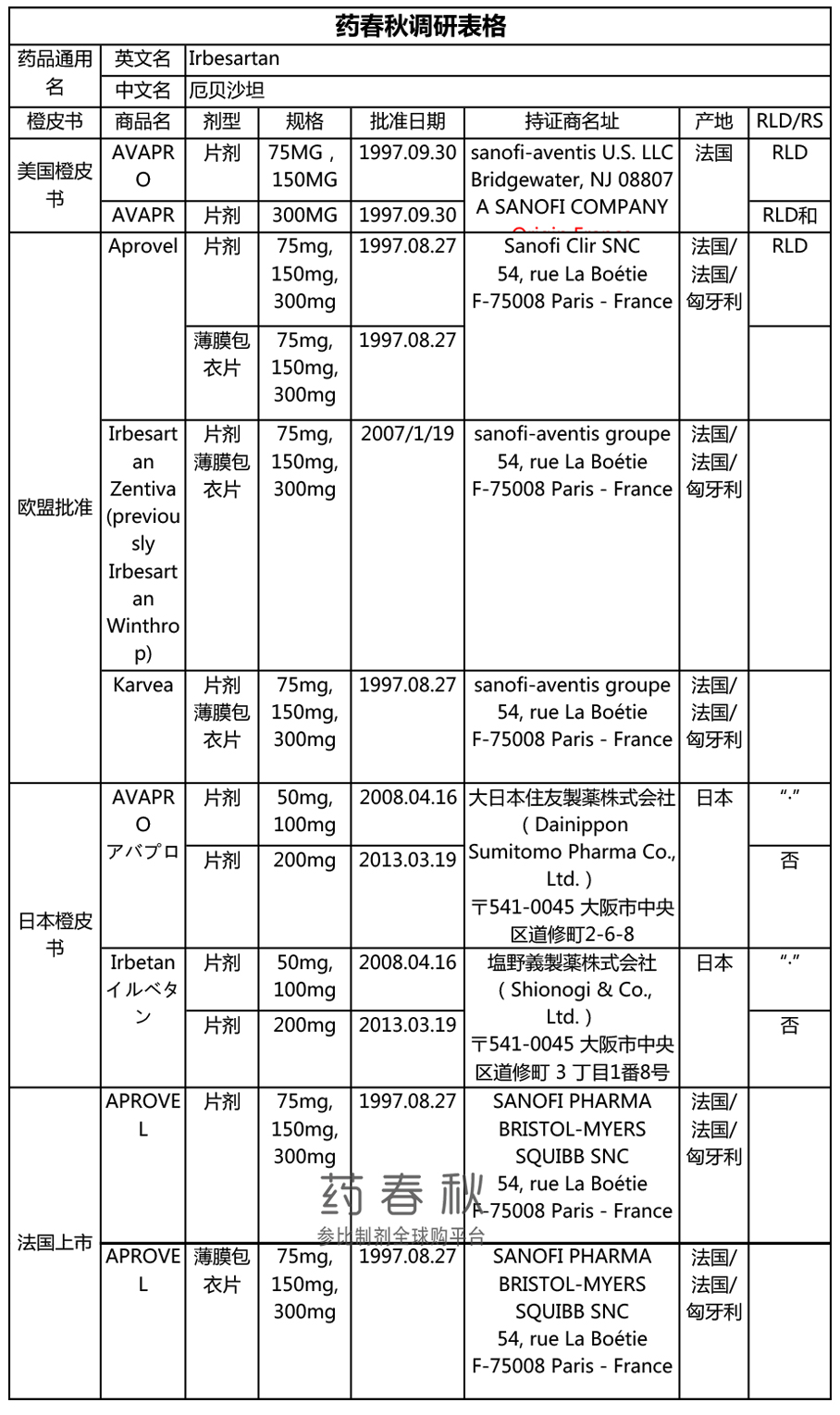
(来源|药春秋网站)
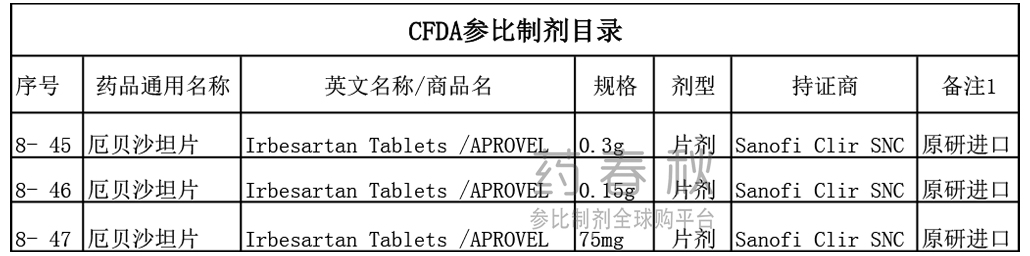
CFDA参比制剂目录
CFDA选用原研进口赛诺菲的三个规格75mg、150mg、300mg的产品作为厄贝沙坦片的参比制剂。
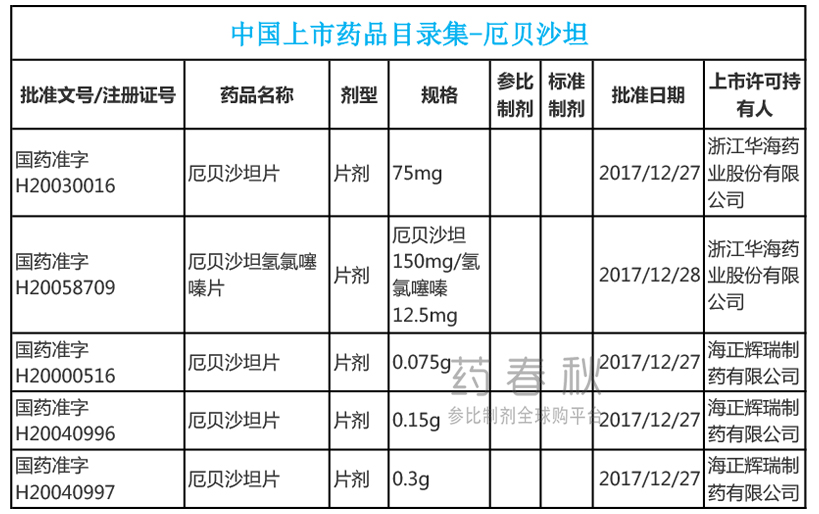
中国上市药品目录
华海药业和海正辉瑞的厄贝沙坦片,均以“在美国上市回国内申报”的方式,成为首批通过一致性评价的药品。
(参考:CFDA2017年第100号文,在欧盟、美国或日本批准上市的仿制药已在中国上市并采用同一生产线同一处方工艺生产的,申请人提交境外上市申报的生物等效性研究、药学研究数据等技术资料,审评通过后,视同通过一致性评价。)
临床试验登记信息
恒瑞和赛诺菲(杭州)的厄贝沙坦片150mg规格的BE试验已完成,对该品种一致性评价进展带来很大的推动。长澳制药、扬子江、为康制药仍在进行中。
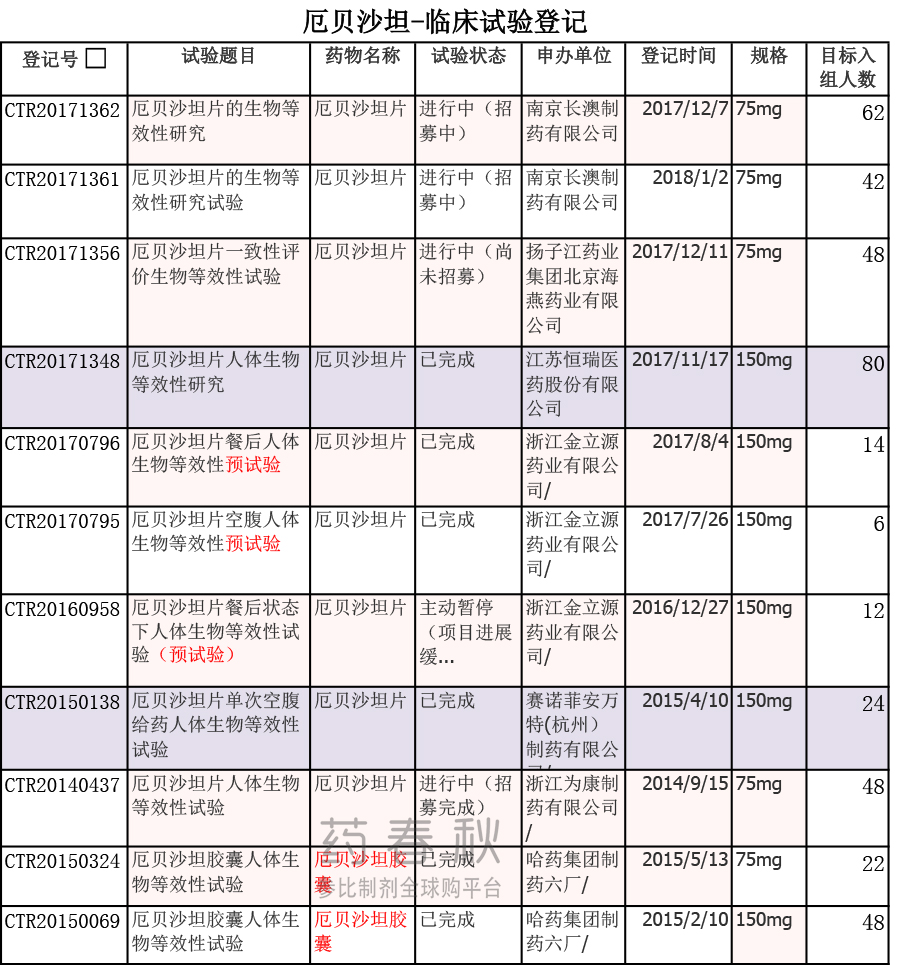
(来源|CDE网站 2018.02.09)
CDE注册申请
近日,赛诺菲(杭州)和恒瑞已向CDE提交了补充申请,处于审评审批状态,若其中一家能顺利通过,则厄贝沙坦通过一致性评价的前三家企业名额已满。
(根据CFDA 2017 年第 100 号公告:同品种药品通过一致性评价的生产企业达到 3 家以上的,在药品集中采购等方面不再选用未通过一致性评价的品种。)
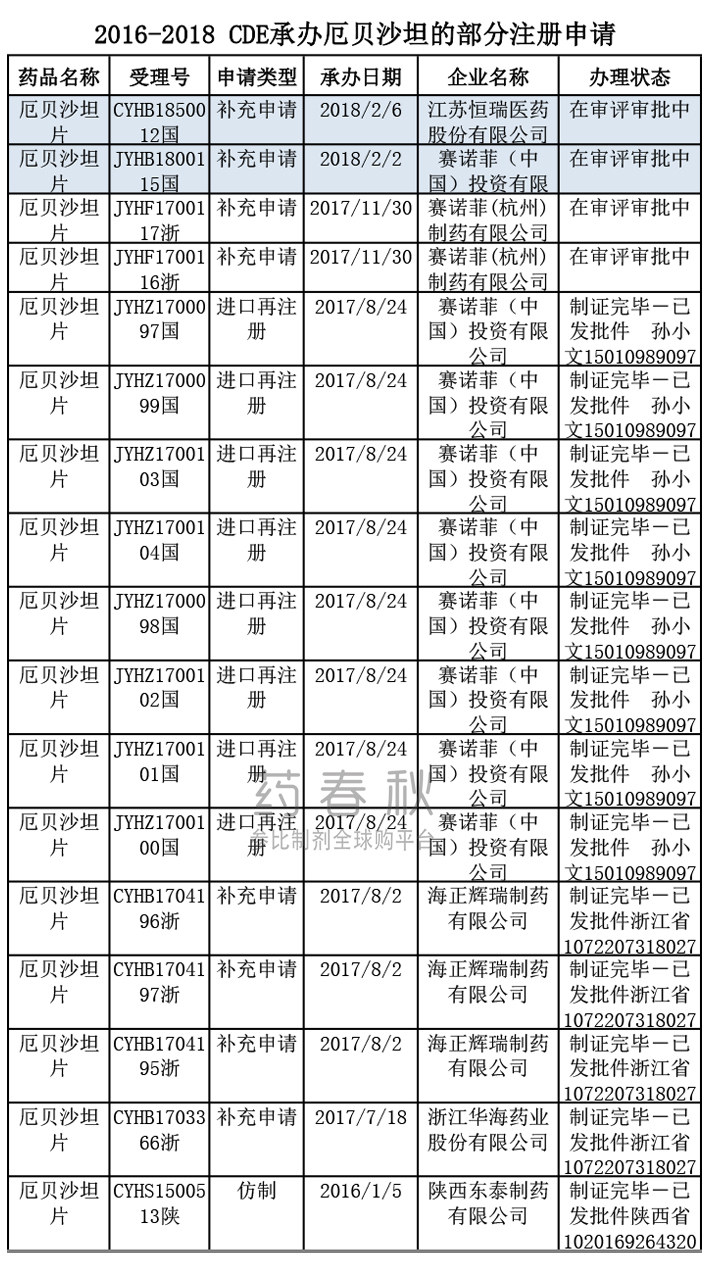
(来源|CDE网站 2018.02.08)
分析&总结
速度之争,不如规格恰逢
海正和华海,虽然率先通过了厄贝沙坦的一致性评价,但此两家原市场占有率极低,如何利用这先发优势扩大市场是重点;海正的三个规格75mg、150mg、300mg都通过了一致性评价,而华海仅有75mg规格通过,该规格的市场份额远小于150mg规格。
恒瑞势头很好,原市场份额排第三,若其150mg规格产品能通过一致性评价,极有可能挤占排第二的润都制药厄贝沙坦胶囊剂份额。
由于一致性评价政策对国产仿制药的扶持,赛诺菲的份额将会受到一定程度冲击,但也不会有断崖式的下滑,从药品中标价格(贵州)看,赛诺菲的150mg*7片的价格是30.1元,恒瑞150*7片的价格是7元,虽然两者相差较大,但本品价格原本就不高,预测价格的差距不会对赛诺菲造成很大的影响。赛诺菲仍会是本品市场的王者。
系列阅读:
替诺福韦:仿制前仆后继,原研降价来抵!
阿卡波糖调研:市场三分,后来者可赶上乎?
苯磺酸氨氯地平调研数据:参比明确,表现活跃!
氯雷他定调研数据:进口过期,何处寻参比?
重磅品种:硫酸氢氯吡格雷片调研数据
药春秋干货:阿昔洛韦片市场调研数据
参比制剂采购咨询,请联系客服~~
客服 黄姑娘 18138751390
客服 林妹妹 18011892830
客服 卜才女 18011892831



