本周新闻要点
第一条.国家医保局正式公布“2019国家医保目录调整方案”,提出了优先考虑癌症、罕见病、重大疾病、高血压糖尿病治疗用药、儿童用药急抢救用药等,同时提到不能纳入目录的品种如滋补药品、濒危野生动植物药品、预防性疫苗、避孕药物等,另外很有可能调出此类药物:撤销/吊销批文、禁止生产销售、临床价值不高的药物。
第二条.国家局对浙江省局的“关于京新瑞舒伐他汀钙原料生产销售合法性问题”的复函,提到原辅包批文有效期届满,可继续使用在原药品,如果用于其他制剂,应完成登记或与制剂申请一同申报。
一致性评价方面
本周通过一致性评价品种有2家:远大医药的碳酸氢钠片,为第三家通过评价,距离第一、二家通过评价的企业(上周通过),仅仅相隔数日;成都倍特的头孢克肟胶囊脱颖而出,首家通过一致性评价。
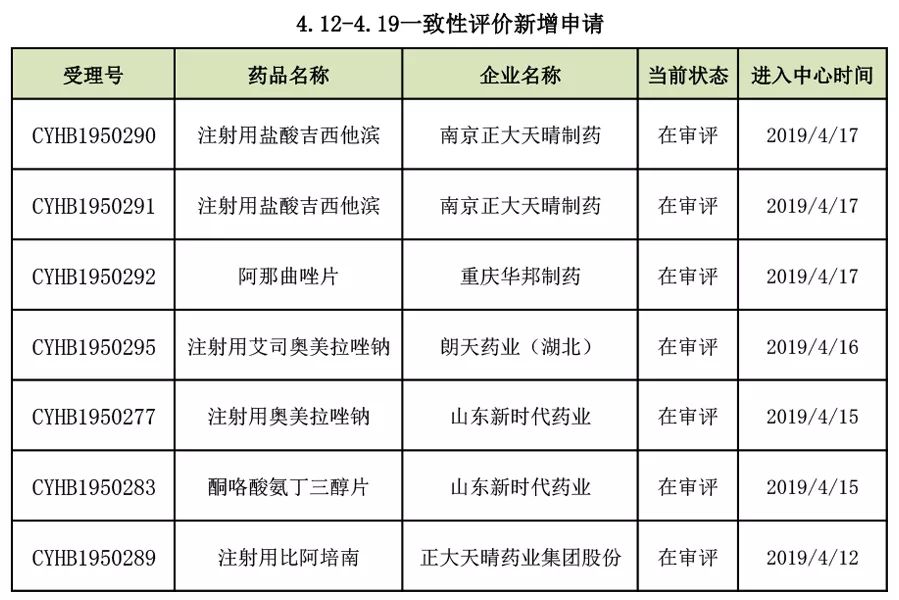
本周(4.12-4.19)新增一致性评价申请7条,其中5条是注射剂的申请,这信息是否表示着,注射剂的一致性评价评价大潮不知不觉已来到身边了呢?
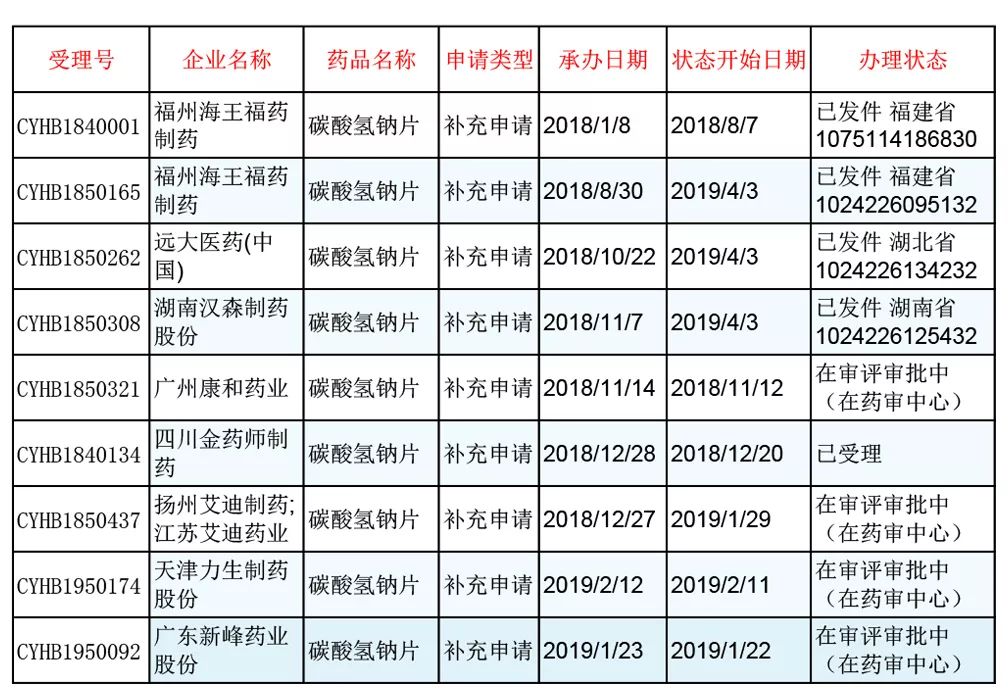
碳酸氢钠片-远大医药
碳酸氢钠片用于缓解胃酸过多引起的胃痛、胃灼热感(烧心)、反酸,已进入2017年国家甲类医保目录和2018年国家基药目录。
就在上周,海王福药和湖南汉森制药两家企业几乎同一时间通过一致性评价,加上本周的远大医药,猝不及防便集齐了前三家,还有5家企业已提交一致性评价申请。虽然一致性评价之后,本品仍免不了恶战,可相比于此前158家获批生产厂家的混战,门槛都提升了许多,本品的质量水平会有大大提升。
头孢克肟胶囊-成都倍特
头孢克肟为第三代头孢类广谱抗生素药物,并属国家医保乙类药物,适用于治疗敏感菌所致的呼吸、泌尿和胆道等部位的感染。
目前国内上市的头孢克肟有片剂、分散片、干混悬剂、胶囊、咀嚼片、颗粒多种剂型,其中胶囊剂获批厂家有24家,其中3家已提交一致性评价申请,成都倍特首家过评。
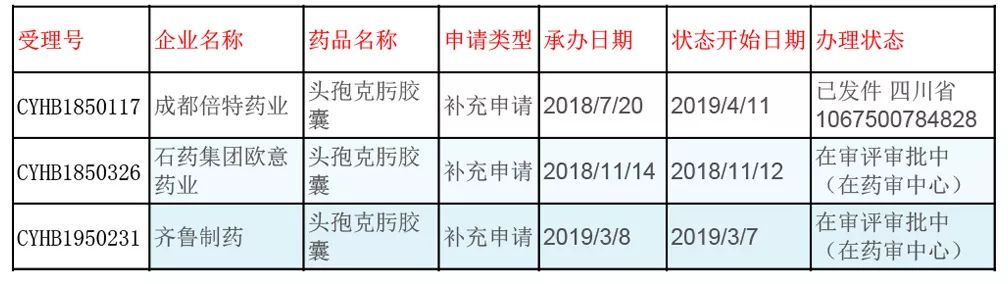
本品是成都倍特第4个通过一致性评价的品种,另外已过评的还有氟康唑胶囊、头孢呋辛酯片、富马酸替诺福韦二吡呋酯片。
截止目前,CDE承办的一致性评价申请共1063条,其中注射剂250条,涉及87个品种。
本周新增5条注射剂一致性评价申请,来自4个品种:注射用盐酸吉西他滨、注射用艾司奥美拉唑钠、注射用奥美拉唑钠、注射用比阿培南。
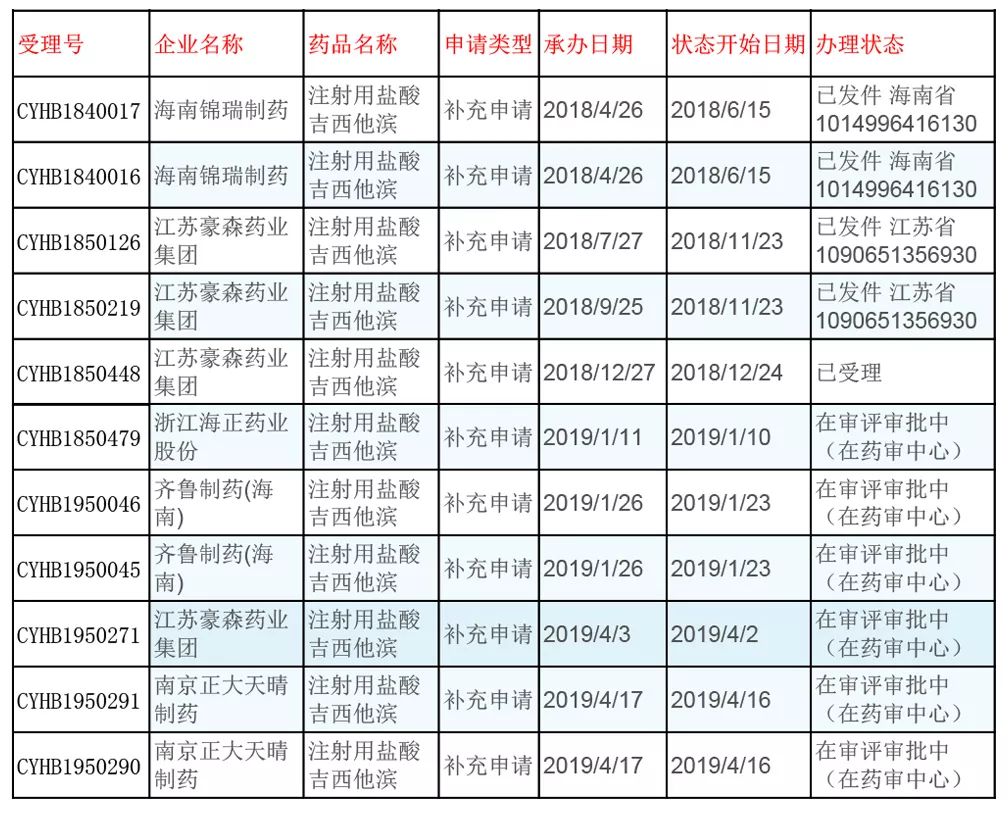
注射用盐酸吉西他滨-正大天晴
吉西他滨为嘧啶类抗肿瘤药物,临床上适应症有——局部晚期或已转移的非小细胞肺癌;局部晚期或已转移的胰腺癌;不能切除的、局部复发或转移性乳腺癌等。
本品获批生产厂家18家,提交一致性评价申请的有5家。
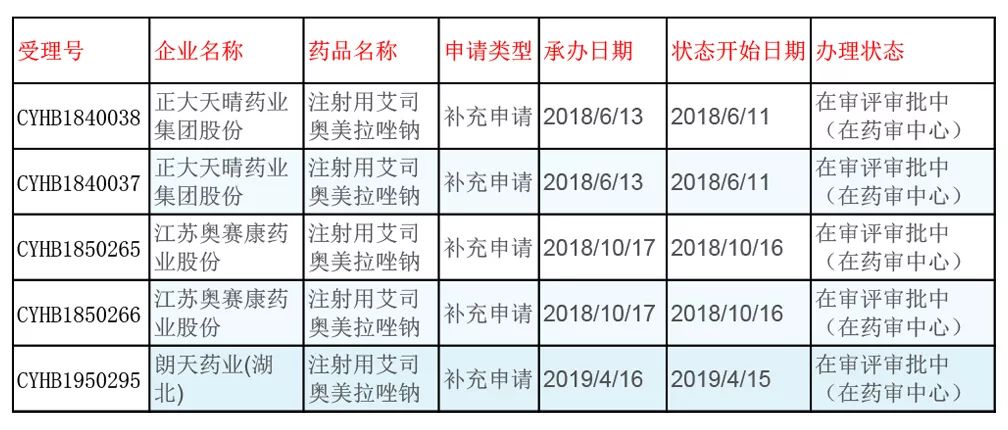
注射用艾司奥美拉唑钠-朗天药业
目前,国内上市的质子泵抑制剂主要是奥美拉唑、泮托拉唑、兰索拉唑、艾司奥美拉唑等,预计年销售规模超200亿元。
艾司美拉唑最先由阿斯利康公司研发,2000年以埃索美拉唑镁的口服制剂在瑞典上市,之后开发了注射用埃索美拉唑钠。
朗天药业的注射用艾司奥美拉唑钠(商品名:新蓝雪)于2018年4月获批上市,一年的时间里一鼓作气申报一致性评价,成为该企业在消化领域上市的重磅产品。
目前该品已提交一致性评价申请企业还有正大天晴、江苏奥赛康。
注射用奥美拉唑钠-山东新时代药业
作为首个应用于临床的质子泵抑制剂,奥美拉唑曾经是全球重磅炸弹药物,至今在国内市场,仍然是处方量最大的PPI类药物。
本品已获批生产厂家有106家,目前提交一致性评价申请的企业只有3家:江苏奥赛康、广州一品红制药山东新时代药业。
一致性评价俨然成了过度重复、产量过剩品种的出路。
注射用比阿培南-正大天晴
比阿培南是新一代碳青霉烯类抗生素,具有抗菌谱广、药动学特性优良并对肾脱氢肽酶-I稳定等优点,能满足了我国市场对抗耐药性药物的迫切需求,为患者带来更多样的选择。
正大天晴与上海医工院于2002年起合作开展该项目的研究开发工作,攻克了合成路线长、难度大、能耗高,关键中间体制备成本高、后处理繁琐,结晶工艺不稳定,质量难以控制等多项技术难点,于2008年获得比阿培南及其制剂的新药证书和生产批件。
目前国内该品获批生产厂家有6家,正大天晴率先提交一致性评价申请,保持在该品在研发和产业化方面的优势地位。
注射剂一致性评价,已逐渐转到主车道上,且不少企业已开上了快车道。未来已来。
THE END



