试点3+1年后,被誉为给我国创新型企业带来一场“及时雨”的药品上市许可人(Marketing Authorization Holder,MAH)制度,即将在今年12月开始全面推行。
4年来,业界和监管方都寄望以MAH制度来打破创新药研发和生产的生态格局,如今,试点结束,如何在MAH试点案例中判断创新药未来的发展方向?未来全面推行又将面临哪些机遇与挑战?
MAH是什么?意义是什么?
MAH制度是指将上市许可与生产许可分离的管理模式。在这种机制下,上市许可和生产许可相互独立。上市许可持有人可以将产品委托给不同的生产商生产,药品的安全性、有效性和质量可控性均由上市许可人对公众负责。
和记黄埔医药资深副总裁吴振平博士认为:“MAH制度的核心就是鼓励新药研发,让精于研发者专注于研发、精于生产者做好生产。”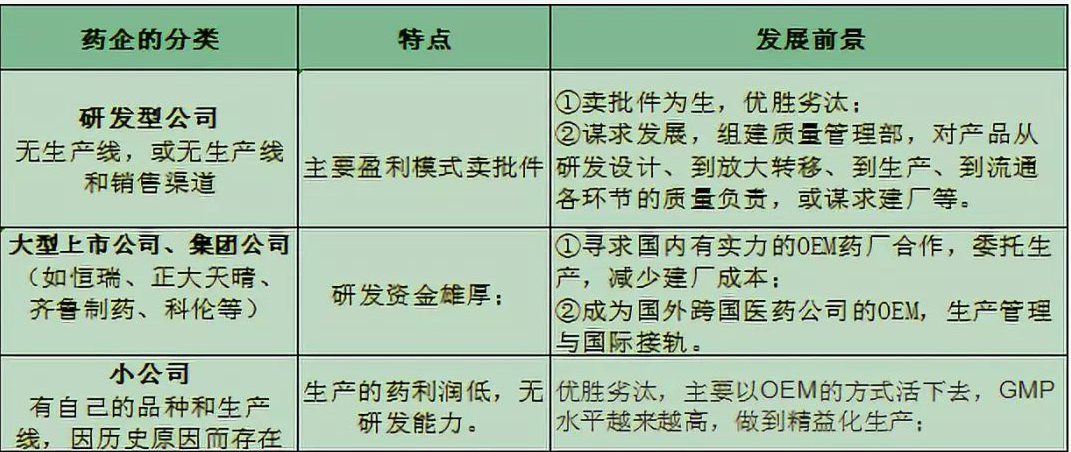
在我国,药企主要分为以上三类。2016 年以前,我国的药品注册制度是上市许可与生产许可“捆绑式”模式,研发方若要把药品批准文号掌握在自己手中,需建设生产线,拿到生产许可批文。因此一些不少新药研发团队面对“投资建厂”这一门槛望而却步,只有将相关药品技术转让给生产企业,俗称,忍痛卖“青苗”!
在吴振平博士看来,MAH项目归项目,生产线归生产线的管理模式,对于不少创新型企业而言,无疑是一场“及时雨”。主要有以下好处:
● 激发暂时不具备生产条件的各类企业的创新药研发积极性和创新活力;
● 降低研发投入附带的生产设施建设投入门槛,让研发型企业通过委托生产的方式实现创新药的迅速产业化,让制药企业通过收购等方式获得创新药实现产品上市。
MAH试点3+1年 激活一池春水
● 2015年11月,中国开始试行上市许可人制度(MAH);
● 2016年6月6日,药品上市许可持有人制度试点自方案印发之日正式启动,北京、天津、河北、上海、江苏、浙江、福建、山东、广东、四川等10个省(市)撸起袖子加油干!
● 2018年11月4日,MAH试点原计划结束日延期1年至2019年11月4日。
● 2019年8月26新《药品管理法》宣布MAH将于12月1日起在正式在全国推广实施。
在这试点过程中,MAH试点品种陆续获批,可谓各地开花。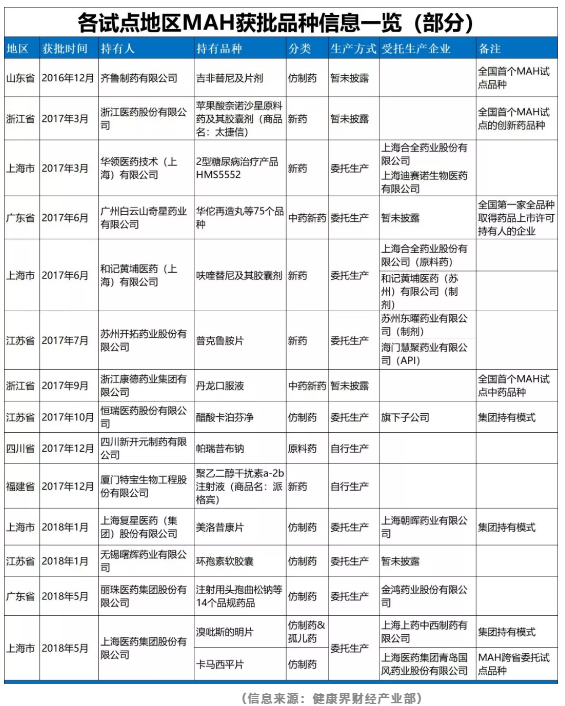
截至2019年7月底,国家药品监督管理局宣布药品上市许可持有人数据库统计指出,共纳入上市许可持有人品种3239个(以药品批准文号计),上市许可持有人主体156个。
而早前据《中国新药杂志》统计,截至2018年9月底,10 个试点省( 市) 药品注册申请人共提出持有人申请1118 件,全面涵盖了《试点方案》规定的行政区域、主体类型和试点药品范围。
试点药品范围覆盖情况中,新药占42.6% ; 按与原研药质量和疗效一致的新标准研发的仿制药占 44.8%,而从地域分布情况来看,江苏、广东和山东 3 个省占比超过一半。
可以看到,MAH为各大创新药企带来了多元选择,进一步释放了我国医药产业的创新活力。
MAH活化多元化产业
全面推进MAH制度,需要进一步解放思想、创新理念、健全制度、完善机制。同时,MAH制度要求我们认识到尊重市场、尊重企业选择、尊重监管规律的重要性,也是我国新修订的药品管理法中重点关注的内容。
同时,随着MAH 的实施,也会给一些新的保险公司、第三方评估、委托合同专业的评估等服务性机构增长空间,只要各方更好地磨合和适应,完善MAH市场机制,就能真正做好为更多创新药开辟绿色通道,早日造福更多的中国患者。
▲信息来源:新浪医药



